Công thức phân tử : CH4.
Phân tử khối: 16.
I. TRẠNG THÁI TỰ NHIÊN, TÍNH CHẤT VẬT LÍ
- Trong tự nhiên, metan có nhiều trong các mỏ khí (khí thiên nhiên), trong mỏ dầu (khí đồng hành), trong các mỏ than (khí mỏ than), trong bùn ao (khí bùn ao), khí biogaz. Khí metan được sinh ra trong điều kiện các chất hữu cơ bị vi sinh vật phân hủy trong điều kiện hiếm khí.(có rất ít khí oxi).
- Metan là chất khí, không màu, không mùi, nhẹ hơn không khí và tan rất ít trong nước.
II. CẤU TẠO PHÂN TỬ
-Trong phân từ metan chỉ có liên kết đơn, công thức cấu tạo của metan:
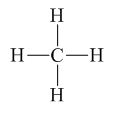
- Giữa nguyên tử C và nguyên tử H chỉ có 1 liên kết những liên kết như vậy gọi là liên kết đơn.
- Ta thấy trong phân tử mêtan có 4 liên kết đơn.
III. TÍNH CHẤT HÓA HỌC
1. Tác dụng với oxi:
- Khi đốt metan cháy trong khí oxi thì tạo thành khí CO2 và H2O, tỏa nhiều nhiệt.
CH4(k) + 2O2(k) -> CO2(k) + 2H2O(h) ( điều kiện nhiệt độ)
2. Tác dụng với clo khi có ánh sáng:
Tiến hành thí nghiệm cho hỗn hợp khí metan và clo phản ứng với nhau trong một bình kín, dưới điều kiện có chiếu sáng.
Hiện tượng: Ban đầu hỗn hợp khí có màu vàng, sau một thời gian thì màu vàng nhạt dần rồi mất đi.
CH4 + Cl2 -> HCl + CH3Cl (clo metan) ( điều kiện ánh sáng)
- Ở phản ứng này, nguyên tử H của metan được thay thế bởi nguyên tử Cl, vì vậy được gọi là phản ứng thế.
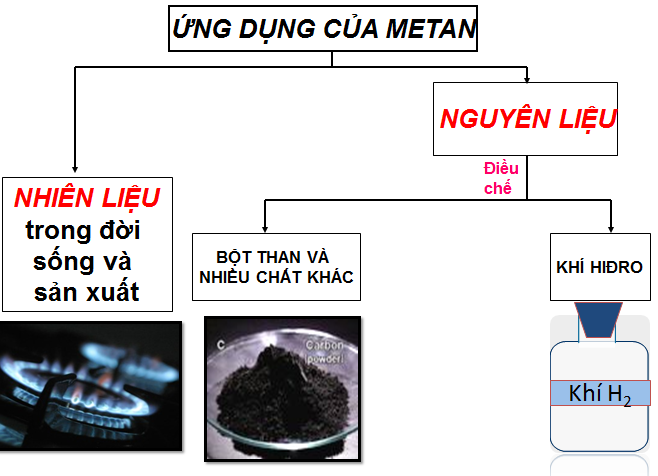
IV. ỨNG DỤNG
- Metan cháy tỏa nhiều nhiệt nên được đùng làm nhiên liệu.
- Metan là nguyên liệu dùng điều chế hiđro theo phản ứng : CH4(k) + H2O -> CO2(k) + H2(k)
- Metan còn được dùng để điều chế bột than và nhiều chất khác.

.jpg)
.jpg)




.jpg)
.jpg)










