I. HẠT NHÂN NGUYÊN TỬ
1. Điện tích hạt nhân
a) Proton mang điện tích +1, nếu hạt nhân có Z proton thì điện tích của hạt nhân bằng Z+ và số đơn vị điện tích hạt nhân bằng Z.
b) Nguyên tử trung hòa về điện nên số proton của hạt nhân = số electron của nguyên tử. Z = P = E.
VD: Nguyên tử Na có số đơn vị điện tích hạt nhân là 11 thì số hạt proton = 11 và số electron = 11.
2. Số khối
a) Số khối A = Z + N (tổng số hạt proton và notron). VD: Số khối của hạt nhân nguyên tử Na, A = 11 + 12 = 23.
b) Số đơn vị điện tích hạt nhân Z và số khối A đặc trưng cho hạt nhân và cũng đặc trưng cho nguyên tử vì khi biết Z và A sẽ biết được số proton, số notron và số electron. VD: Nguyên tử Al có A = 27, Z = 13 nên số proton = số electron = 13, số notron = A - Z = 14.
II. NGUYÊN TỐ HÓA HỌC
1. Định nghĩa
Nguyên tố hóa học là những nguyên tử có cùng điện tích hạt nhân.
2. Số hiệu nguyên tử
Số đơn vị điện tích hạt nhân nguyên tử của một nguyên tố được gọi là số hiệu nguyên tử của nguyên tố đó, kí hiệu Z.
3. Kí hiệu nguyên tử
Nguyên tử X, có số khối A và điện tích hạt nhân Z được kí hiệu là: AZX (số khối A ở trên và điện tích Z ở dưới). VD: 2311Na.
III. ĐỒNG VỊ
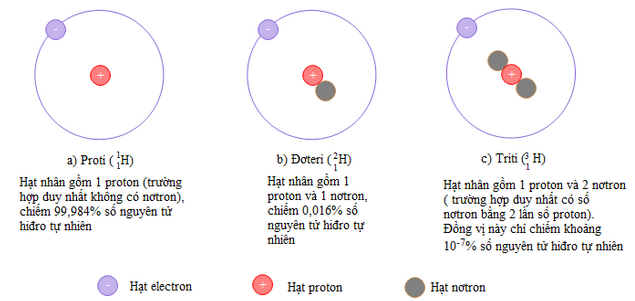
Các đồng vị của cùng một nguyên tố hóa học là những nguyên tử có cùng số proton nhưng khác nhau về số notron, do đó số khối A của chúng khác nhau. VD: nguyên tố H có 3 đồng vị là 11H (Proti), 21H (Đơteri) và 31H (Triti).
IV. NGUYÊN TỬ KHỐI VÀ NGUYÊN TỬ KHỐI TRUNG BÌNH CỦA CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tử khối
Nguyên tử khối là khối lượng tương đối của nguyên tử.
Nguyên tử khối của một nguyên tử cho biết khối lượng của nguyên tử đó nặng gấp bao nhiêu lần đơn vị khối lượng nguyên tử.
Khối lượng của một nguyên tử bằng tổng khối lượng của proton, notron và electron trong nguyên tử đó, nhưng do khối lượng của electron quá nhỏ so với hạt nhân nên có thể bỏ qua. Vì vậy, khối lượng của nguyên tử coi như bằng tổng khối lượng của các ptron và notron trong hạt nhân nguyên tử.
Nguyên tử khối coi như bằng số khối (khi không cần độ chính xác cao).
Ví dụ: Nguyên tử khối của P là 31 vì Z = 15 và N = 16.
2. Nguyên tử khối trung bình
- Hầu hết các nguyên tố hóa học là hỗn hợp của nhiều đồng vị với tỉ lệ phần trăm số nguyên tử xác định => nguyên tử khối của các nguyên tố có nhiều đồng vị là nguyên tử khối trung bình của hỗn hợp các đồng vị có tính đến tỉ lệ phần trăm số nguyên tử tương ứng.
- Giả sử nguyên tố X có 2 đồng vị A và B. kí hiệu A,B đồng thời là nguyên tử khối của 2 đồng vị, tỉ lệ phần trăm số nguyên tử tương ứng là a và b. Công thức tính nguyên tử khối trung bình:
.png)

.jpg)
.jpg)




.jpg)
.jpg)










