A. Natri Hiđroxit
I. TÍNH CHẤT VẬT LÝ
- Natri hidroxit NaOH là chất rắn không màu, hút ẩm mạnh, tan nhiều trong nước và tỏa nhiệt.
- Dung dịch NaOH có tính nhờn làm bục vải, giấy và ăn mòn da.Khi sử dụng natri hiđroxit phải hết sức cẩn thận
II. TÍNH CHẤT HÓA HỌC
NaOH là bazơ tan và có các tính chất hóa học của một bazơ tan:
- Làm đổi màu chất chỉ thị ( phenolphtalein, quì tím ).
- Tác dụng với axit.
- Tác dụng với oxit axit.
- Tác dụng với dung dịch muối.
1. Đổi màu chất chỉ thị
Dung dịch NaOH làm quì tím chuyển sang màu xanh, phenolphtalein không màu thành màu đỏ.
2. Tác dụng với axit
Dung dịch NaOH tác dụng với axit, tạo thành muối và nước (phản ứng trung hòa)
3. Tác dụng với oxit axit
Dung dịch NaOH tác dụng với oxit axit, tạo thành muối và nước
III. ỨNG DỤNG
- Natri hiđroxit có nhiều ứng dụng rộng rãi trong đời sống và trong công nghiệp.
- Nó được dùng trong:
- Sản xuất xà phòng, chất tẩy rửa, bột giặt.
- Sản xuất tơ nhân tạo.
- Sản xuất giấy.
- Sản xuất nhôm (làm sạch quặng nhôm trước khi sản xuất).
- Chế biến dầu mỏ và nhiều ngành công nghiệp hoá chất khác.
IV. SẢN XUẤT NATRI HIĐROXIT
Natri hiđroxit được sản xuất bằng phương pháp điện phân dung dịch NaCl bào hoà. Thùng điện phản có màng ngăn giữa cực âm và cực dương. Người ta thu được khí hiđro ở cực âm, khí clo ở cực dương và dung dịch NaOH trong thùng điện phân
1. NaOH là một chất kiềm, có những tính chất hoả học sau: đổi màu chất chỉ thị, tác dụng với axit, oxif axit và muối.
2. NaOH là hoá chất quan trọng của nhiều ngành công nghiệp.
3. NaOH được điều chế bằng phương pháp điện phân (có màng ngăn) dung dịch NaCl bão hoà, sản phẩm là dung dịch NaOH, khí H2 và Cl2
B. CANXI HIDROXIT - THANG pH
I. TÍNH CHẤT
1. Pha cha dung dịch Canxi hidroxit
Dung dịch Ca(OH)2 có tên gọi thông thường là nước vôi trong.
Hòa tan một ít vôi tôi Ca(OH)2 trong nước, ta được một chất lỏng màu trắng có tên gọi là vôi nước hoặc vôi sữa. Lọc vôi nước ta được một chất lỏng trong suốt, không màu là dung dịch Ca(OH)2
2. Tính chất hóa học
Dung dịch Ca(OH)2 có tính chất hóa học của bazo tan
a. Làm đổi màu chất chỉ thị
dd Ca(OH)2 đổi màu quỳ tím thành xanh, hoặc đổi màu dd phenolptalein không màu thành màu hồng
b. Tác dụng với Axit (tạo muối và nước)
Phương trình hóa học:
H2SO4 + Ca(OH)2 → CaSO4 + 2H2O
2HCl + Ca(OH)2 → CaCl2 + 2H2O
c. Tác dụng với oxit axit (tạo muối + nước)
Tuỳ theo tỉ lệ số mol của Ca(OH)2 với số SO2 mà có thể tạo muối trung hoà và nước, muối axit hoặc cả hai
muối.
Phương trình hóa học:
Ca(OH)2 + CO2 → CaCO3 + H2O
Ca(OH)2 + SO2 → CaSO3 + H2O
d. Tác dụng với dung dịch muối (Học ở bài 9)
3. Ứng dụng của Canxi hidroxit
Làm vật liệu xây dựng
Khử chua đất trồng trọt
Khử độc các chất thải trong công nghiệp, diệt trùng chất thải sinh hoạt và xác chết động vật
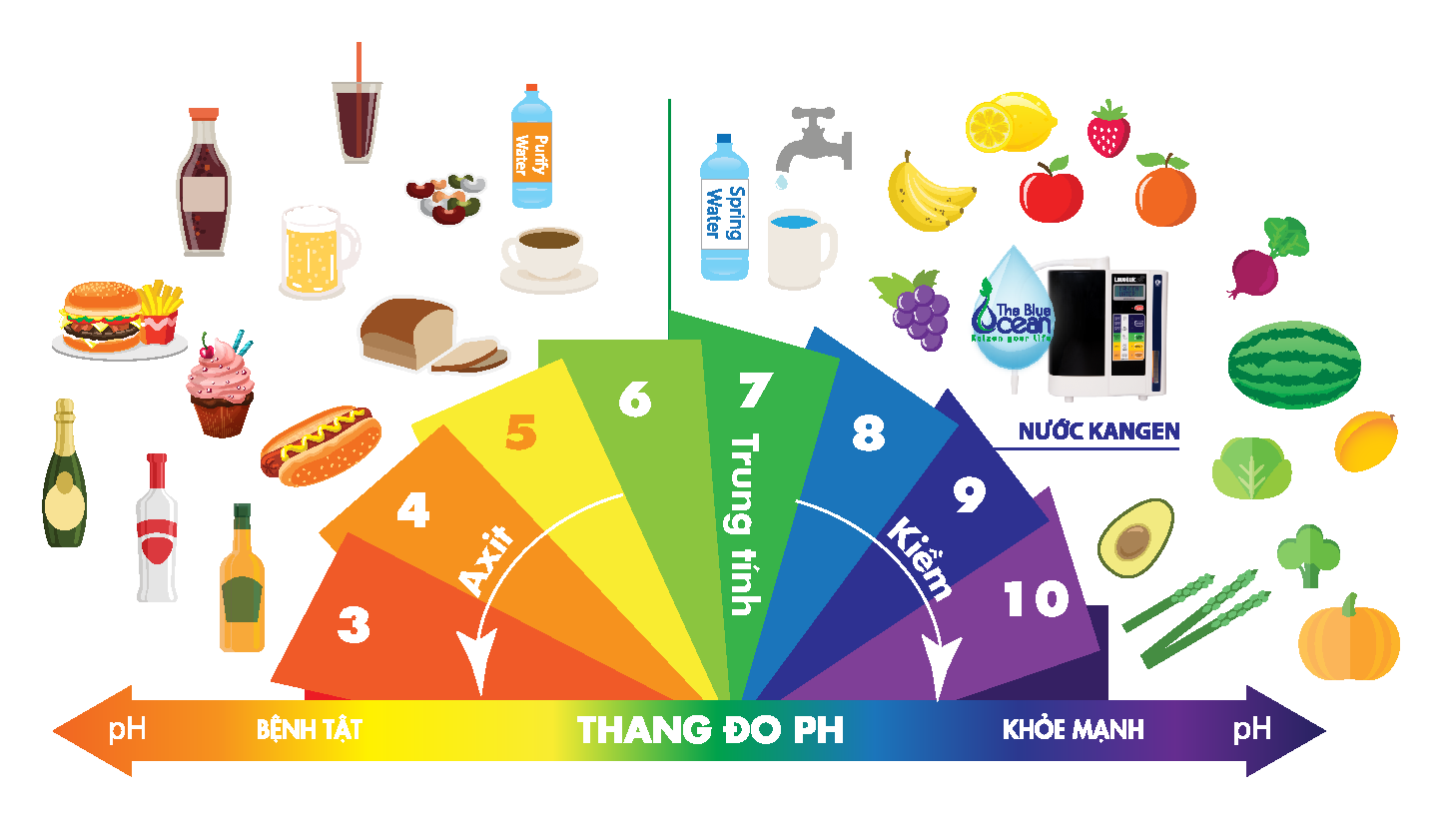
II. THANG pH
Thang pH dùng để biểu thị độ axit hoặc độ bazơ của dung dịch
Nếu pH = 7 thì dung dịch là trung tính
Nếu pH > 7 thì dung dịch có tính bazơ ⇒ Nếu pH càng lớn, độ bazơ của dung dịch càng lớn và ngược lại
Nếu pH < 7 thì dung dịch có tính axit ⇒ Nếu pH càng nhỏ, độ axit của dung dịch càng lớn và ngược lại
1. Dung dịch canxi hidroxit là dung dịch kiềm (đổi màu chất chỉ thị, tác dụng với oxit axit, axit và muối). Canxi hidroxit có nhiều ứng dụng trong đời sống và sản xuất.
2 pH của một dung dịch cho biết độ axit hoặc độ bazo của dung dịch : Trung tính : pH = 7; Tinh axit : pH < 7: Tính bazơ : pH >7

.jpg)
.jpg)




.jpg)
.jpg)










