1. Số oxi hóa, sự oxi hóa và sự khử
Trong Hóa hữu cơ, những phản ứng có sự thay đổi số oxi hóa cũng được gọi là phản ứng oxi hóa - khử, cách tính số oxi hóa cho mỗi nguyên tử cũng tuân theo các quy tắc như đối với các hợp chất vô cơ. Tuy nhiên, vì tiêu điểm của sự chú ý tập trung vào phân tử chất hữu cơ (chứ không phải đồng đều cho cả tác nhân vô cơ) nên để xác định đâu là sự oxi hóa, đâu là sự khử người ta thường xem xét sự thay đổi số oxi hóa ở phân tử hợp chất hữu cơ trước và sau phản ứng.
Bởi vì phản ứng hữu cơ thường có liên quan tới một vài nguyên tử C trong phân tử nên để xác định sự oxi hóa và sự khử, người ta làm như sau:
- Tính số oxi hóa của tất cả các nguyên tử cacbon bị biến đổi cấu tạo khi chuyển từ chất đầu sang sản phẩm phản ứng.
- Lấy tổng số oxi hóa của các nguyên tử C biến đổi ở phân tử sản phẩm trừ đi tổng số oxi hóa của các nguyên tử C biến đổi ở phân tử chất đầu
Nếu hiệu số thì ta gọi đó là sự oxi hóa (hợp chất hữu cơ)
Nếu hiệu số thì ta nói đó là sự khử (hợp chất hữu cơ)
Nếu hiệu số thì phản ứng không phải là oxi hóa cũng không phải là khử.
Thí dụ 1:
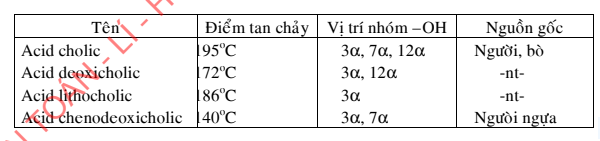
Thí dụ 2:
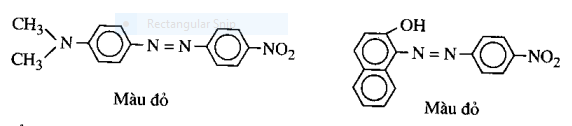
Thí dụ 3:
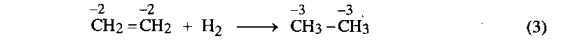

Từ các thí dụ trên cho thấy, các phản ứng thế, cộng tách... có thể là hoặc không phải là phản ứng oxi hóa - khử. Tuy có những đặc điểm riêng, nhưng về hình thức vẫn có sự tương đồng giữa phản ứng oxi hóa - khử ở hợp chất hữu cơ và vô cơ. Cụ thể là: ở các quá trình oxi hóa hợp chất hữu cơ, , nghĩa là số oxi hóa tăng; còn ở các quá trình khử, hiệu số , nghĩa là số oxi hóa giảm.
2. Cân bằng phản ứng oxi hóa - khử trong hóa học hữu cơ
Đối với các phản ứng đơn giản, chỉ cần nhận xét và cân bằng theo phương pháp bình thường. Đối với những phản ứng phức tạp hơn, cần sử dụng phương pháp thăng bằng electron hoặc phương pháp thăng bằng ion - electron
Thí dụ : Hãy viết phương trình phản ứng oxi hóa toluen bằng dung dịch KMnO4 tạo thành kali benzoat và mangan dioxit.
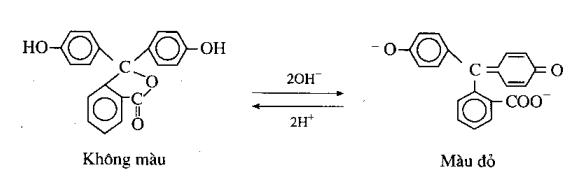
Tiếp theo phải cân bằng số nguyên tử K, O, H với chú ý rằng phản ứng xảy ra trong dung dịch nước, nên chỉ có thể dùng H2O để điều chỉnh số nguyên tử O và H cho đạt cân bằng. Khi đó ta thu được phương trình sau:
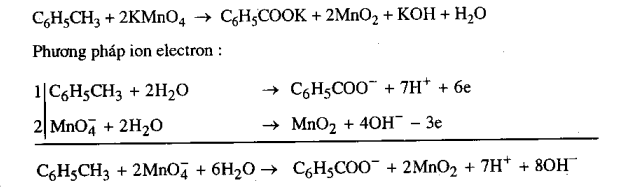
Tiếp theo cần đưa thêm 2K+ vào mỗi vế và chuyển 7H+ + 8OH- thành 7H2O + OH- rồi giản ước 6H2O ở cả hai vế ta thu được phương trình
![]()

.jpg)
.jpg)




.jpg)
.jpg)










