I. VỊ TRÍ VÀ CẤU HÌNH ELECTRON NGUYÊN TỬ
Cấu hình e: 1s2 2s2 2p6 3s2 3p3.
Ví trí: Z = 15, chu kì 3, nhóm VA
Hoá trị có thể có của P: 5 và 3
II. TÍNH CHẤT VẬT LÝ
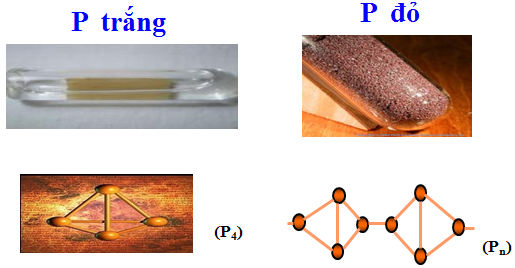
Photpho tạo thành hai dạng thù hình quan trọng: photpho trắng và photpho đỏ.
1. Photpho trắng: Chất rắn màu trắng, mềm, phát quang trong bóng tối, dễ nóng chảy, khi rơi vào da thì gây bỏng nặng, dễ bốc cháy ở nhiệt độ > 40oC. Photpho trắng không tan trong nước nên người ta bảo quản nó bằng cách ngâm trong nước.
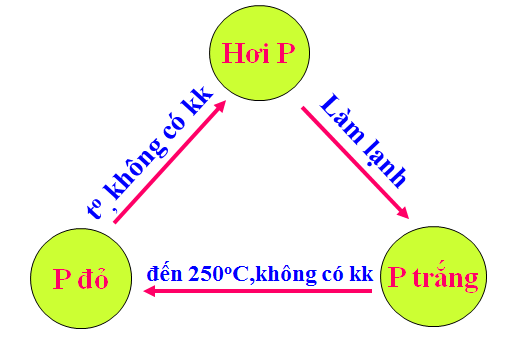
2. Photpho đỏ: Chất rắn có màu đỏ, dễ hút ẩm, chảy rữa, bền trong không khí và nhiệt độ thường. Chỉ bốc chấy ở nhiệt độ >250oC
- Trong hai dạng thù hình photpho trắng hoạt động hơn photpho đỏ.
III. TÍNH CHẤT HÓA HỌC
Photpho là phi kim tương đối hoạt động. Photpho trắng hoạt động hóa học mạnh hơn photpho đỏ. Trong các hợp chất, photpho có số oxi hóa là -3, +3, +5
Do đó, khi tham gia phản ứng hóa học photpho thể hiện tính oxi hóa hoặc tính khử
1. Tính oxi hoá
2P + 3Ca .png) Ca3P2
Ca3P2
2. Tính khử
Khi tác dụng với phi kim hoạt động và những chất oxi hoá mạnh.-
- Với oxi:
5O2 (dư) + 4P ![]() 2P2O5 (Điphotpho pentaoxit)
2P2O5 (Điphotpho pentaoxit)
3O2 (thiếu) + 4P ![]() 2P2O3 (Điphotpho trioxit)
2P2O3 (Điphotpho trioxit)
- Với clo:
5Cl2 (dư) +2P ![]() 2PCl5 (photpho pentaclorua)
2PCl5 (photpho pentaclorua)
3Cl2 (thiếu) + 2P ![]() 2PCl3 (photpho triclorua)
2PCl3 (photpho triclorua)
IV. ỨNG DỤNG

Ứng dụng của photpho
V. TRẠNG THÁI TỰ NHIÊN

Hai khoáng vật chính của photpho
VI. SẢN XUẤT
Trong công nghiệp, photpho đỏ được sản xuất bằng cách nung hỗn hợp quặng photphorit (hoặc apatit), cát và than cốc ở 1200oC trong lò điện.
Lào Cai là một trong những tỉnh giàu tài nguyên khoáng sản nhất Việt Nam với 35 loại khoáng sản khác nhau. Trong đó có nhiều loại khoáng sản như apatít, đồng, sắt, graphít, nguyên liệu cho gốm, sứ, thuỷ tinh,… với trữ lượng lớn nhất cả nước.

.jpg)
.jpg)




.jpg)
.jpg)










